Echilibrul acido-bazic - echilibrul pH - raportul dintre acid și alcali. Instrucțiuni pentru hârtie indicatoare - instrucțiuni pentru hârtie de turnesol pentru măsurarea pH-ului
Temporar stocul este epuizat
Se așteaptă primirea
Hârtie de turnesol (test pH) 80 benzi de la 1 la 14 Cod pH: 309
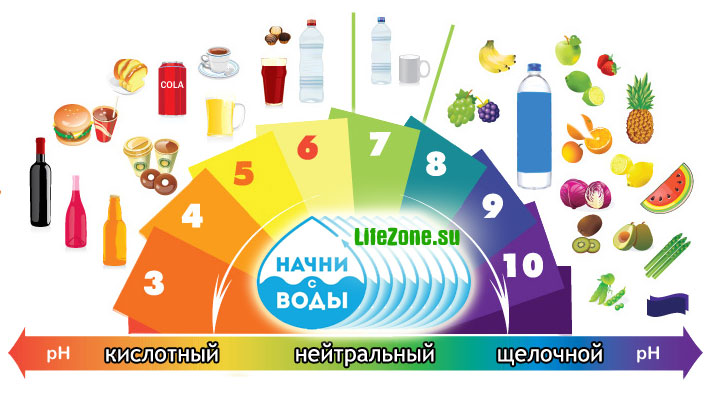
Pachet de 80 benzi de turnesol pentru testarea pH-ului. Există o diagramă de culori cu pH-ul pe ambalaj.
Pasul de măsurare - 1
Cu ajutorul benzilor de testare a pH-ului, puteți determina echilibrul acido-bazic (pH) al oricărui mediu lichid fără a părăsi casa. Testele noastre de pH au cel mai mare interval de măsurare, și anume de la 1 la 14, și sunt potrivite atât pentru nevoi medicale, cât și pentru cele casnice, de exemplu:
Pentru a determina calitatea laptelui,
Pentru a determina aciditatea apei, urinei,
Când testați pH-ul pentru acvarii și piscine,
La monitorizarea apelor potabile, naturale și alte ape.
Mod de utilizare: scufundați banda de testare în test
soluția timp de 1-2 secunde, apoi îndepărtați-o și comparați după 15 secunde
colorarea unei benzi indicatoare cu o scară de culori.
Scara este reprezentată de valorile: 1 2 3 4 5 6 7 8 9 10 11 12 13 14
Nivelul pH-ului, numit și pH, caracterizează concentrația ionilor de hidrogen. Într-un mediu neutru, valoarea pH-ului este de 7, în medii acide - mai puțin de 7, iar în medii alcaline - peste 7
Țara producătorului: China

În orice soluție se numește echilibru acido-bazic ( KShchR), deși fiziologii cred că este mai corect să numim acest raport starea acido-bazică.
KShchR se caracterizează printr-un indicator special de pH (puterea Hidrogenului - „puterea hidrogenului”), care arată numărul de atomi de hidrogen dintr-o soluție dată.
La un pH de 7,0, se vorbește de un mediu neutru.
Cu cât pH-ul este mai scăzut- subiecte mediu mai acid(de la 6,9 la 0).
Un mediu alcalin are un nivel ridicat de pH (de la 7,1 la 14,0).
Corpul uman pe 70% constă din apă, De aceea apa este unul dintre cei mai importanți constituenți ai săi.
Corpul uman are un anumit raport acido-bazic, caracterizat prin indicele pH (hidrogen).
Valoarea pH-ului depinde de raportul dintre ionii încărcați pozitiv (formând un mediu acid) și ionii încărcați negativ (formând un mediu alcalin).
Organismul se străduiește constant să echilibreze acest raport, menținând un nivel de pH strict definit.
Când echilibrul este perturbat, pot apărea multe boli grave.
 Verificați echilibrul acido-bazic cu benzile de testare pentru pH.
Verificați echilibrul acido-bazic cu benzile de testare pentru pH.
Este foarte important să acordați atenție modificării în timp a nivelului pH-ului mediului intern al corpului și, dacă este necesar, să luați măsuri urgente.
Cu ajutorul benzilor de testare a pH-ului, puteți determina cu ușurință, rapid și exact nivelul pH-ului fără a părăsi casa.
Cel mai bun moment pentru a măsura nivelul pH-ului este 1 oră înainte de masă sau 2 ore după masă.
Verificați nivelul pH-ului de 2 ori pe săptămână de 2-3 ori pe zi.
Necunoașterea nivelului pH-ului poate duce la consecințe triste.
A) Aciditate crescută în organism
Un dezechilibru în pH-ul corpului la majoritatea oamenilor se manifestă sub formă de aciditate crescută (o afecțiune Acidoza).
În această stare, organismul nu absoarbe minerale precum calciul, sodiul, potasiul și magneziul, care, din cauza acidității în exces, sunt excretate din organism.
Organele vitale suferă din cauza lipsei de minerale.
Acidoza nedepistată la timp poate dăuna organismului în mod imperceptibil, dar în mod constant timp de câteva luni și chiar ani.
Abuzul de alcool duce adesea la acidoză.
Acidoza poate apărea ca o complicație a diabetului.
Acidoza poate provoca următoarele probleme:
B) Conținut crescut de alcali în organism
Cu un conținut crescut de alcali în organism, și această stare se numește Alcaloza, precum și în cazul acidozei, absorbția mineralelor este perturbată.
Alimentele sunt digerate mult mai lent, ceea ce permite trecerea toxinelor din tractul gastrointestinal în sânge.
Conținutul crescut de alcali în organism este periculos și greu de corectat.
De regulă, este rezultatul utilizării medicamentelor care conțin alcali.
Un conținut crescut de alcali poate provoca:
Valoarea pH-ului urinei
Rezultatele testului de pH al urinei arată cât de bine absoarbe organismul minerale precum calciul, sodiul, potasiul și magneziul.
Aceste minerale sunt numite „acide amortizoare” deoarece reglează nivelul de aciditate din organism.
Dacă aciditatea este prea mare, organismul nu produce acid.
Ar trebui să neutralizeze acidul.
Pentru a face acest lucru, organismul începe să împrumute minerale de la diferite organe, oase și așa mai departe. pentru a neutraliza excesul de acid care începe să se acumuleze în țesuturi.
Astfel, nivelul de aciditate este reglat.
Mineralele sunt folosite pentru neutralizarea acizilor
Timp de 7 ani, un studiu a fost efectuat la Universitatea din California (San Francisco), unde au fost examinate 9 mii de femei.
Rezultatele au arătat că la constant nivel ridicat aciditate, oasele devin casante.
Experții care au efectuat acest experiment sunt siguri că majoritatea problemelor femeilor de vârstă mijlocie sunt asociate cu consumul excesiv de carne și cu lipsa consumului de alimente vegetale.
Prin urmare, organismul nu are de ales decât să ia calciu din propriile oase și, cu ajutorul lui, să regleze nivelul pH-ului.
(American Journal of Clinical Nutrition).
Valoarea pH-ului salivei

De asemenea, este rațional să cunoaștem nivelul pH-ului salivei.
Rezultatele testelor arată activitatea enzimelor din tractul digestiv, în special a ficatului și a stomacului.
Acest indicator oferă o idee despre activitatea atât a întregului organism în ansamblu, cât și a sistemelor sale individuale.
Unele persoane pot avea hiperaciditate atât în urină, cât și în salivă – caz în care avem de-a face cu „aciditate dublă”.
Valoarea pH-ului sângelui

pH-ul sângelui este una dintre cele mai rigide constante fiziologice ale corpului.
În mod normal, acest indicator poate varia în interiorul 7.3b - 7.42.
O schimbare a acestui indicator cu cel puțin 0,1 poate duce la o patologie severă.
Cu o schimbare a pH-ului sângelui cu 0,2, se dezvoltă o comă, cu 0,3, o persoană moare.
Păstrați echilibrul corect al pH-ului pentru o sănătate bună
Organismul este capabil să absoarbă și să stocheze în mod corespunzător mineralele și substanțele nutritive doar la nivelul adecvat al echilibrului acido-bazic.
Este în puterea ta să-ți ajuți corpul să primească, mai degrabă decât să piardă, nutrienți.
De exemplu, fier Pot fi fi asimilat organism la pH 6,0 - 7,0 , A iod- la pH 6,3 - 6,6 .
Corpul nostru folosește acidul clorhidric pentru a descompune alimentele.
În procesul de activitate vitală a organismului, sunt necesare atât produse de degradare acide, cât și alcaline, iar primii se formează de 20 de ori mai mult decât cei din urmă.
Prin urmare, sistemele de apărare ale organismului, care asigură invarianța ASC-ului său, sunt „ajustate” în primul rând pentru a neutraliza și a excreta, în primul rând, produsele de degradare acide.
Principalele mecanisme de menținere a acestui echilibru sunt:
Este în interesul dumneavoastră să mențineți echilibrul corect al pH-ului.
Chiar și „cel mai bun” program pe bază de plante nu va funcționa eficient dacă echilibrul pH-ului este dezactivat.
Cum gestionează organismul nivelul de acid?
Supliment alimentar pentru normalizarea echilibrului pH-ului în organism:
 Reface deficitul de enzime digestive Reface deficitul de enzime digestive Îmbunătățește digestia și absorbția nutrienți Normalizează funcționarea organelor sistem digestiv Reglați nivelul de acid clorhidric din stomac Normalizează microflora tractului gastrointestinal Au efect antiinflamator Reglează echilibrul acido-bazic în organism 120 capsule | 21,56 USD |
Valoarea pH-ului și influența acesteia asupra calității apei potabile.
Ce este pH-ul?
pH("potentia hydrogeni" - puterea hidrogenului, sau "pondus hydrogenii" - greutatea hidrogenului) este o unitate de măsură a activității ionilor de hidrogen în orice substanță, exprimând cantitativ aciditatea acesteia.
Acest termen a apărut la începutul secolului al XX-lea în Danemarca. Indicele pH a fost introdus de chimistul danez Soren Petr Lauritz Sorensen (1868-1939), deși predecesorii săi au și afirmații despre o anumită „putere a apei”.
Activitatea hidrogenului este definită ca logaritmul zecimal negativ al concentrației ionilor de hidrogen, exprimat în moli pe litru:
pH = -log
Pentru simplitate și comoditate, pH-ul a fost introdus în calcule. pH-ul este determinat de raportul cantitativ dintre ionii H+ și OH- din apă, care se formează în timpul disocierii apei. Se obișnuiește să se măsoare nivelul pH-ului pe o scară de 14 cifre.
Dacă apa are un conținut redus de ioni de hidrogen liberi (pH mai mare de 7) în comparație cu ionii de hidroxid [OH-], atunci apa va avea reacție alcalină, și cu un conținut crescut de ioni H + (pH mai mic de 7) - reacție acidă. În apă distilată perfect pură, acești ioni se vor echilibra reciproc.
mediu acid: >
mediu neutru: =
mediu alcalin: >
Când concentrațiile ambelor tipuri de ioni într-o soluție sunt aceleași, se spune că soluția este neutră. În apă neutră, pH-ul este 7.
Când se dizolvă în apă, diverse substanțe chimice acest echilibru se modifică, rezultând o modificare a valorii pH-ului. Când se adaugă acid în apă, concentrația de ioni de hidrogen crește, iar concentrația de ioni de hidroxid scade în consecință, când se adaugă alcali, dimpotrivă, conținutul de ioni de hidroxid crește, iar concentrația de ioni de hidrogen scade.
Indicatorul de pH reflectă gradul de aciditate sau alcalinitate al mediului, în timp ce „aciditatea” și „alcalinitatea” caracterizează conținutul cantitativ al substanțelor din apă care pot neutraliza alcalii și, respectiv, acizii. Ca analogie, putem da un exemplu cu temperatura, care caracterizează gradul de încălzire al unei substanțe, dar nu și cantitatea de căldură. Prin scufundarea mâinii în apă, putem spune dacă apa este rece sau caldă, dar, în același timp, nu vom putea determina câtă căldură este în ea (adică, relativ vorbind, cât timp se va răci această apă).
pH-ul este considerat unul dintre cei mai importanți indicatori ai calității apei potabile. Arată echilibrul acido-bazic și influențează modul în care substanța chimică și procese biologice. În funcție de valoarea pH-ului, se pot modifica viteza reacțiilor chimice, gradul de coroziune al apei, toxicitatea poluanților etc. Bunăstarea, starea de spirit și sănătatea noastră depind direct de echilibrul acido-bazic al mediului înconjurător al corpului nostru.
Omul modern trăiește într-o zonă poluată mediu inconjurator. Mulți oameni cumpără și consumă alimente făcute din semifabricate. În plus, aproape fiecare persoană este expusă la stres în fiecare zi. Toate acestea afectează echilibrul acido-bazic al mediului organismului, deplasându-l spre acizi. Ceaiul, cafeaua, berea, bauturile carbogazoase scad pH-ul din organism.
Se crede că un mediu acid este una dintre principalele cauze ale distrugerii celulelor și ale leziunilor tisulare, a dezvoltării bolilor și a procesului de îmbătrânire și a creșterii agenților patogeni. Într-un mediu acid, materialul de construcție nu ajunge în celule, membrana este distrusă.
În exterior, starea echilibrului acido-bazic al sângelui unei persoane poate fi judecată după culoarea conjunctivei sale din colțurile ochilor. Cu un echilibru acido-bazic optim, culoarea conjunctivei este roz aprins, dar dacă o persoană are o alcalinitate crescută a sângelui, conjunctiva capătă o culoare roz închis, iar odată cu creșterea acidității, culoarea conjunctivei devine roz pal. Mai mult, culoarea conjunctivei se schimbă deja la 80 de secunde după utilizarea substanțelor care afectează echilibrul acido-bazic.
Organismul reglează pH-ul fluidelor interne, menținând valorile la un anumit nivel. Echilibrul acido-bazic al organismului este un anumit raport de acizi și alcalii care contribuie la funcționarea sa normală. Echilibrul acido-bazic depinde de menținerea unor proporții relativ constante între apele intercelulare și cele intracelulare din țesuturile corpului. Dacă echilibrul acido-bazic al fluidelor din organism nu este menținut în mod constant, funcționarea normală și păstrarea vieții vor fi imposibile. Prin urmare, este important să controlezi ceea ce consumi.

Echilibrul acido-bazic este indicatorul nostru de sănătate. Cu cât suntem mai acizi, cu atât îmbătrânim mai repede și ne îmbolnăvim mai mult. Pentru funcționarea normală a tuturor organe interne Nivelul pH-ului din organism ar trebui să fie alcalin, în intervalul de la 7 la 9.
pH-ul din corpul nostru nu este întotdeauna același - unele părți sunt mai alcaline, iar altele sunt mai acide. Organismul reglează și menține homeostazia pH-ului doar în anumite cazuri, cum ar fi pH-ul sângelui. Nivelul pH-ului rinichilor și al altor organe, al căror echilibru acido-bazic nu este reglat de organism, este afectat de alimentele și băuturile pe care le consumăm.
pH-ul sângelui
Nivelul pH-ului din sânge este menținut de organism în intervalul 7,35-7,45. Indicator normal pH-ul sângelui uman este considerat a fi 7,4-7,45. Chiar și o ușoară abatere a acestui indicator afectează capacitatea sângelui de a transporta oxigen. Dacă pH-ul sângelui crește la 7,5, acesta transportă cu 75% mai mult oxigen. Cu o scădere a pH-ului sângelui la 7,3, este deja dificil pentru o persoană să se ridice din pat. La 7.29, poate intra în comă, dacă pH-ul sângelui scade sub 7,1, persoana moare.
pH-ul sângelui trebuie menținut într-un interval sănătos, astfel încât organismul folosește organe și țesuturi pentru a-l menține constant. În consecință, nivelul pH-ului sângelui nu se modifică din cauza consumului de apă alcalină sau acidă, dar țesuturile și organele corpului folosite pentru ajustarea pH-ului sângelui își modifică pH-ul.
pH-ul rinichilor
Parametrul de pH al rinichilor este influențat de apă, alimente și procesele metabolice din organism. Alimente acide (ex. produse din carne, produse lactate etc.) și băuturile (sucuri îndulcite, băuturi alcoolice, cafea etc.) duc la niveluri scăzute ale pH-ului la nivelul rinichilor deoarece organismul excretă excesul de aciditate prin urină. Cu cât pH-ul urinei este mai scăzut, cu atât este mai greu pentru rinichi să lucreze. Prin urmare, încărcătura acidă pe rinichi de la astfel de alimente și băuturi se numește potențial încărcare acido-renală.
Utilizarea apei alcaline aduce beneficii rinichilor - are loc o creștere a nivelului pH-ului urinei, încărcarea acidă a organismului este redusă. Creșterea pH-ului urinei crește pH-ul corpului în ansamblu și elimină rinichii de toxinele acide.
pH-ul stomacului
Un stomac gol nu conține mai mult de o linguriță de acid gastric produs la ultima masă. Stomacul produce acid după cum este necesar atunci când mănâncă alimente. Stomacul nu eliberează acid atunci când o persoană bea apă.
Este foarte util să bei apă pe stomacul gol. pH-ul crește în același timp până la nivelul de 5-6. Un pH crescut va avea un efect antiacid ușor și va duce la o creștere a probioticelor benefice (bacteriile benefice). Creșterea pH-ului stomacului crește pH-ul organismului, ceea ce duce la o digestie sănătoasă și ameliorarea simptomelor indigestiei.
pH-ul grăsimii subcutanate
Tesuturile grase ale organismului au un pH acid deoarece in ele se depun acizi in exces. Organismul trebuie să stocheze acidul în țesuturile adipoase atunci când acesta nu poate fi îndepărtat sau neutralizat în alte moduri. Prin urmare, schimbarea pH-ului corpului către partea acidă este unul dintre factorii excesului de greutate.
Efectul pozitiv al apei alcaline asupra greutății corporale este că apa alcalină ajută la eliminarea excesului de acid din țesuturi, deoarece ajută rinichii să funcționeze mai eficient. Acest lucru ajută la controlul greutății, deoarece cantitatea de acid pe care organismul trebuie să o „pastreze” este mult redusă. Apa alcalină îmbunătățește, de asemenea, rezultatele unei diete sănătoase și ale exercițiilor fizice, ajutând organismul să facă față excesului de acid produs de țesutul gras în timpul pierderii în greutate.
Oase
Oasele au un pH alcalin deoarece sunt alcătuite în mare parte din calciu. pH-ul lor este constant, dar dacă sângele are nevoie de ajustare a pH-ului, calciul este luat din oase.
Beneficiul pe care apa alcalină îl aduce oaselor este de a le proteja prin reducerea cantității de acid cu care trebuie să se confrunte organismul. Studiile au arătat că consumul de apă alcalină reduce resorbția osoasă - osteoporoza.
pH-ul ficatului
Ficatul are un pH ușor alcalin, care este afectat atât de mâncare, cât și de băutură. Zahărul și alcoolul trebuie descompuse în ficat, iar acest lucru duce la exces de acid.
Beneficiile apei alcaline pentru ficat sunt prezența antioxidanților în astfel de apă; s-a constatat că apa alcalină îmbunătățește activitatea a doi antioxidanți localizați în ficat, care contribuie la o purificare mai eficientă a sângelui.
pH-ul corpului și apa alcalină
Apa alcalină permite părților corpului care mențin pH-ul sângelui să funcționeze mai eficient. Creșterea nivelului pH-ului în părțile corpului responsabile de menținerea pH-ului sângelui va ajuta aceste organe să rămână sănătoase și să funcționeze eficient.
Între mese, vă puteți ajuta corpul să-și echilibreze pH-ul bând apă alcalină. Chiar și o mică creștere a pH-ului poate avea un impact uriaș asupra sănătății.
Potrivit cercetărilor oamenilor de știință japonezi, pH-ul apei potabile, care este în intervalul 7-8, crește speranța de viață a populației cu 20-30%.
În funcție de nivelul pH-ului, apa poate fi împărțită în mai multe grupuri:
ape puternic acide< 3
ape acide 3 - 5
ape usor acide 5 - 6,5
ape neutre 6,5 - 7,5
ape usor alcaline 7,5 - 8,5
ape alcaline 8,5 - 9,5
ape foarte alcaline > 9,5
În mod obișnuit, nivelul pH-ului apei potabile de la robinet se află în intervalul în care nu afectează în mod direct calitatea apei de consumator. În apele râurilor pH-ul este de obicei între 6,5-8,5, în precipitațiile atmosferice 4,6-6,1, în mlaștini 5,5-6,0, în apele mării 7,9-8,3.
OMS nu oferă nicio valoare recomandată din punct de vedere medical pentru pH. Se știe că la pH scăzut, apa este foarte corozivă, iar la niveluri înalte(pH>11) apa capătă un săpun caracteristic, un miros neplăcut și poate irita ochii și pielea. De aceea, pentru apa potabilă și menajeră, nivelul pH-ului în intervalul de la 6 la 9 este considerat optim.
|
|||||||||||||||||||||||||||||||||||||||||||||||



Interesant de știut: Biochimistul german OTTO WARBURG, care a primit Premiul Nobel pentru Fiziologie sau Medicină în 1931, a demonstrat că lipsa oxigenului (un pH acid<7.0) в тканях приводит к изменению нормальных клеток в злокачественные.
Omul de știință a descoperit că celulele canceroase își pierd capacitatea de a se dezvolta într-un mediu saturat cu oxigen liber cu o valoare a pH-ului de 7,5 și mai mare! Aceasta înseamnă că atunci când fluidele din organism devin acide, dezvoltarea cancerului este stimulată.
Adepții săi din anii 60 ai secolului trecut au demonstrat că orice floră patogenă își pierde capacitatea de a se înmulți la pH = 7,5 și peste, iar sistemul nostru imunitar poate face față cu ușurință oricăror agresori!
Pentru a păstra și menține sănătatea, avem nevoie de apă alcalină adecvată (pH=7,5 și peste). Acest lucru vă va permite să mențineți mai bine echilibrul acido-bazic al fluidelor corporale, deoarece principalele medii de viață au o reacție ușor alcalină.
Deja într-un mediu biologic neutru, organismul poate avea o capacitate uimitoare de a se vindeca singur.

Nu știu de unde să ajung apa corecta ? Voi solicita!

Notă:
Apăsând butonul " A sti» nu conduce la nicio cheltuială și obligație financiară.
Esti doar obțineți informații despre disponibilitatea apei potrivite în zona dvs,
și obțineți o oportunitate unică de a deveni gratuit membru al clubului oamenilor sănătoși
și obțineți o reducere de 20% la toate ofertele + bonus cumulativ.

Alăturați-vă clubului internațional de sănătate Coral Club, obțineți un card de reducere GRATUIT, posibilitatea de a participa la promoții, un bonus cumulativ și alte privilegii!

Determinând zilnic pH-ul salivei, poți controla starea corpului tău.
Pentru identificarea acizilor și bazelor.
Pentru un metabolism uman normal este necesar ca echilibrul acido-bazic să fie menținut în anumite limite.
Soluțiile și lichidele în funcție de aciditatea lor sunt luate în considerare:
neutru la pH = 7
acid la pH< 7
alcalin la pH > 7
Aciditatea urinei
Dacă nivelul pH-ului urinei fluctuează între 6,0 - 6,4 dimineața și 6,4 - 7,0 seara, atunci organismul funcționează normal. Cel mai optim nivel este ușor acid, în intervalul 6,4 - 6,5. O valoare a pH-ului urinei sub 5,0 indică aciditatea sa ascuțită, peste 7,5 - reacția sa puternic alcalină.
Reacția urinei determină posibilitatea formării pietrelor: în militar - într-un acid, oxalat - într-un acid neutru, fosfat - într-un mediu mai alcalin. Astfel, de exemplu, pietrele de acid uric nu apar niciodată la un pH al urinei mai mare de 5,5, iar pietrele de fosfat nu se formează niciodată decât dacă urina este alcalină. Cel mai bun moment pentru a măsura nivelul pH-ului este cu 1 oră înainte sau 2 ore după masă.
Verificați nivelul pH-ului de două ori pe săptămână de 2-3 ori pe zi.
Folosind testul de pH Indicator Litmus Paper, puteți monitoriza cu ușurință, rapid și precis răspunsul urinei la o modificare a tipului de dietă, la utilizarea medicamentelor sau a suplimentelor alimentare. Dinamica pozitivă a pH-ului poate servi drept criteriu pentru corectitudinea dietei sau a tratamentului ales.
Aciditatea urinei variaza foarte mult in functie de alimentele luate, de exemplu, consumul de alimente vegetale creste reactia alcalina a urinei.Aciditatea urinei creste daca dieta unei persoane este dominata de alimente din carne bogate in proteine.
Munca fizică grea crește aciditatea urinei.
O creștere a acidității urinei se observă cu o aciditate crescută a stomacului. Aciditatea redusă a sucului gastric nu afectează aciditatea urinei.
Aciditatea urinei se modifică cu multe boli sau afecțiuni ale corpului, astfel încât determinarea acidității acesteia este un factor de diagnostic important.
Aciditatea salivei:
Aciditatea salivei depinde de rata salivației. De obicei, aciditatea salivei umane mixte este de 6,8-7,4 pH, dar la o rată mare de salivare ajunge la 7,8 pH. Aciditatea salivei glandelor parotide este de 5,81 pH, glandele submandibulare - 6,39 pH. La copii, aciditatea medie a salivei mixte este de 7,32 pH.
Masurare optima de la 10:00 la 12:00. Este mai bine să-l măsurați pe stomacul gol, cu două ore înainte sau două ore după masă. Salivația este redusă seara și noaptea.
Pentru a crește salivația, pentru a crește pH-ul salivei, este bine dacă în farfurie este o bucată de lămâie, chiar crește salivația cu percepția vizuală. Mâncarea ar trebui să arate apetisantă, servită pe mâncăruri frumoase, decorată apetisant cu verdeață și/sau/legume, ar trebui, după cum se spune, să mulțumească ochiul! Nu numai saliva curge, ci și sucurile în organism, pregătindu-se pentru procesul de digerare a alimentelor. Aceasta este faza psihică a secreției digestive.
Refluxurile acide gastroesofagiene și faringolaringiene care ajung în cavitatea bucală joacă un rol principal în apariția patologiei bucale. Ca urmare a pătrunderii acidului clorhidric, aciditatea salivei mixte scade sub pH 7,0. Saliva, care are în mod normal proprietăți alcaline, la pH scăzut, în special la valori de 6,2-6,0, duce la demineralizarea focală a smalțului dentar cu apariția eroziunii țesuturilor dentare dure și formarea de carii în acestea - carii. Cantitatea de mucus de pe membrana mucoasă crește, gingiile devin umflate și inflamate.
Odată cu scăderea acidității în cavitatea bucală, aciditatea plăcii scade, ceea ce determină dezvoltarea cariilor.
Bacteriile din gură „înfloresc” în absența aerului. Saliva, bogată în oxigen, împiedică activ reproducerea lor. Respirația urat mirositoare apare atunci când fluxul de saliva încetinește, cum ar fi în timpul somnului. Excitare, foame, rostirea unui monolog lung, respirație pe gură (de exemplu, cu o răceală), stres - usucă cavitatea bucală, ducând la scăderea pH-ului salivei. O scădere a fluxului de salivă apare inevitabil odată cu vârsta.
Puteți conecta o clătire de gură ușor alcalină cu apă cu adaos de sifon și, de asemenea, luând-o în interior între mese, propus de profesorul Ogulov A.T. - pH usor alcalin 7,4-8. Clătirea gurii cu apă sodă apare cu diferite boli inflamatorii ale gingiilor și dinților și cu acidificarea generală a organismului.
Puteți seta pH-ul dorit al apei pentru clătire sau ingerare folosind hârtie indicator de turnesol. Nu pot exista retete cu proportiile potrivite, pentru ca. Apa din fiecare regiune are al ei, având propriul pH. Prin urmare, este necesar să aveți la îndemână hârtie indicatoare.
Aciditatea vaginală
Aciditatea normală a vaginului unei femei variază între 3,8 și 4,4 pH și este în medie de 4,0-4,2 pH.
Aciditatea vaginală în diferite boli:
* vaginoza citolitica: aciditate mai mica de 4,0 pH
* microfloră normală: aciditate de la 4,0 până la 4,5 pH
* vaginita candida: aciditate intre 4,0 si 4,5 pH
* Colpita Trichomonas: aciditate de la 5,0 la 6,0 pH
* vaginoza bacteriana: aciditate mai mare de 4,5 pH
* vaginită atrofică: aciditate mai mare de 6,0 pH
* vaginită aerobă: aciditate mai mare de 6,5 pH
Lactobacilii (lactobacilii) și, într-o măsură mai mică, alți reprezentanți ai microflorei normale sunt responsabili pentru menținerea unui mediu acid și suprimarea creșterii microorganismelor oportuniste în vagin. În tratamentul multor boli ginecologice, restabilirea populației de lactobacili și aciditatea normală iese în prim-plan.
Aciditatea spermatozoizilor
Nivelul normal de aciditate a spermei este între 7,2 și 8,0 pH. Abaterile de la aceste valori nu sunt în sine considerate patologice. În același timp, în combinație cu alte abateri, poate indica prezența unei boli.
O creștere a nivelului pH-ului spermatozoizilor are loc în timpul unui proces infecțios. O reacție puternic alcalină a spermatozoizilor (aciditate de aproximativ 9,0-10,0 pH) indică o patologie a glandei prostatei.
Odată cu blocarea canalelor excretoare ale ambelor vezicule seminale, se observă o reacție acidă a spermatozoizilor (aciditate 6,0-6,8 pH).
Capacitatea de fertilizare a unor astfel de spermatozoizi este redusă. Într-un mediu acid, spermatozoizii își pierd mobilitatea și mor. Dacă aciditatea lichidului seminal devine mai mică de 6,0 pH, spermatozoizii își pierd complet mobilitatea și mor.
aciditatea lacrimilor normal - de la 7,3 la 7,5 pH.
Aciditate în stomac. Aciditate ridicată și scăzută
Aciditatea minimă teoretică posibilă în stomac este de 0,86 pH.
Aciditatea maximă teoretică posibilă în stomac este de 8,3 pH.
Aciditatea normală în lumenul corpului stomacului pe stomacul gol este de 1,5-2,0 pH.
Aciditatea de pe suprafața stratului epitelial orientat spre lumenul stomacului este de 1,5-2,0 pH.
Aciditatea în profunzimea stratului epitelial al stomacului este de aproximativ 7,0 pH. Aciditatea normală în antrul stomacului este de 1,3-7,4 pH.
Cauza multor boli ale tractului digestiv este un dezechilibru în procesele de producere a acidului și neutralizare a acidului. Hipersecreția prelungită a acidului clorhidric sau insuficiența neutralizării acide și, ca urmare, aciditatea crescută în stomac și/sau duoden, provoacă așa-numitele boli dependente de acid. În prezent, acestea includ: ulcer peptic al stomacului și duodenului, boala de reflux gastroesofagian (GERD), leziuni erozive și ulcerative ale stomacului și duodenului în timpul tratamentului cu aspirină sau antiinflamatoare nesteroidiene (AINS), sindromul Zollinger-Ellison, gastrită și gastroduodenită și altele cu aciditate ridicată.
Scăderea acidității se observă în cazul gastritei sau gastroduodenitei anacide sau hipoacide, precum și în cazul cancerului de stomac. Gastrita (gastroduodenita) se numește anacid sau gastrită (gastroduodenită) cu aciditate scăzută, dacă aciditatea în corpul stomacului este de aproximativ 5 sau mai multe unități de pH. Cauza acidității scăzute este adesea atrofia celulelor parietale din membrana mucoasă sau o încălcare a funcțiilor acestora.
aciditate în intestine
Aciditatea normală în bulbul duodenal este de 5,6-7,9 pH. Aciditatea în jejun și ileon este neutră sau ușor alcalină și variază de la 7 la 8 pH. Aciditatea sucului intestinului subțire este de 7,2-7,5 pH. Cu secreție crescută, ajunge la 8,6 pH. Aciditatea secreției glandelor duodenale este de la pH 7 până la 8 pH.
Aciditatea sucului pancreatic este de la 7,5 la 9 pH.
Aciditatea sucului colonului este de 8,5-9,0 pH.
În părțile inferioare ale colonului, valorile pH-ului acidității cresc treptat, atingând o valoare maximă a pH-ului în regiunea joncțiunii rectosigmoidiene.
Aciditatefecaleîn mod normal, de la 6,0 la 8,0 pH.
Aciditatea meconiului (fecalele originale ale nou-născuților)- aproximativ 6 pH.
Aciditatea laptelui matern uman - 6,9-7,5 pH
Aciditatea sângelui
Aciditatea plasmatică a sângelui arterial uman variază între 7,37 și 7,43 pH, cu o medie de 7,4 pH. Echilibrul acido-bazic din sângele uman este unul dintre cei mai stabili parametri, menținând componentele acide și alcaline într-un anumit echilibru în limite foarte înguste. Chiar și o ușoară schimbare de la aceste limite poate duce la o patologie severă. Când este mutat pe partea acidă, apare o afecțiune numită acidoză, iar pe partea alcalină - alcaloză. O modificare a acidității sângelui peste 7,8 pH sau sub 6,8 pH este incompatibilă cu viața.
Aciditatea eritrocitelor este de 7,28-7,29 pH.
Sângele normal revitalizează celulele limfatice capabile să distrugă celulele tumorale. Există multe celule limfatice în corpul uman (de exemplu, celule NK, celule LAK). Unicitatea lor constă în faptul că sunt capabile să distingă celulele normale de cele bolnave și afectate și să le distrugă pe acestea din urmă. Aceasta este funcția sistemului imunitar al corpului uman. Cea mai mare activitate a celulelor limfatice în distrugerea celulelor bolnave se manifestă la pH 7,4. Cu toate acestea, de obicei în jurul celulelor afectate, există un mediu mai acid care împiedică activitatea limfocitelor, care funcționează cel mai bine la un pH ușor alcalin. Consumand alimente care au efect alcalinizant, poti ajusta echilibrul pH-ului in limita a 0,5 unitati, creand un mediu favorabil actiunii limfocitelor si distrugerii celulelor deteriorate sau construite anormal.
Țesutul canceros este mai acid decât țesutul normal, iar organismul îl protejează cu o teacă fibroasă care are un pH alcalin. Dacă continuați să utilizați o dietă acidă, membrana se dizolvă și celulele canceroase sunt eliberate.
O dată pe săptămână, când organismul este acidulat, este indicat să-ți aranjezi zile de vindecare, mâncând doar legume (1,5 kg de legume, împărțit pentru întreaga zi), fierte și uneori crude vara, doar prelucrate termic toamna și iarna) și întotdeauna apă caldă curată.
Destul de putine importanţă pentru a menține un nivel normalpH corpul are și starea de spirit a unei persoane, o dispoziție bună veselă normalizează echilibrul acido-bazic. Razi mai mult!
ATENŢIE! La copierea textului sau a unei părți din text, un link obligatoriu către site
Indicator de hidrogen, pH(lat. pondus hydrogenii- „greutatea hidrogenului”, pronunțată "pash") este o măsură a activității (în soluții foarte diluate, echivalentă cu concentrația) ionilor de hidrogen dintr-o soluție, care exprimă cantitativ aciditatea acesteia. Egal în modul și opus în semn cu logaritmul zecimal al activității ionilor de hidrogen, care este exprimat în moli pe litru:
Istoricul pH-ului.
concept pH introdus de chimistul danez Sorensen în 1909. Indicatorul este numit pH (după primele litere ale cuvintelor latine potentia hydrogeni este puterea hidrogenului sau pondus hydrogeni este greutatea hidrogenului). În chimie, combinația pX de obicei desemnează o valoare care este egală cu lg X, dar cu o scrisoare Hîn acest caz indicați concentrația ionilor de hidrogen ( H+), sau mai bine zis, activitatea termodinamică a ionilor de hidroniu.
Ecuații referitoare la pH și pOH.
Valoarea pH-ului de ieșire.
În apă pură la 25 °C, concentrația ionilor de hidrogen ([ H+]) și ioni de hidroxid ([ Oh− ]) sunt aceleași și egale cu 10 −7 mol/l, acest lucru reiese clar din definiția produsului ionic al apei, egal cu [ H+] · [ Oh− ] și este egal cu 10 −14 mol²/l² (la 25 °C).
Dacă concentrațiile a două tipuri de ioni într-o soluție sunt aceleași, atunci se spune că soluția are o reacție neutră. Când se adaugă un acid în apă, concentrația de ioni de hidrogen crește, iar concentrația de ioni de hidroxid scade; când se adaugă o bază, dimpotrivă, conținutul de ioni de hidroxid crește, iar concentrația de ioni de hidrogen scade. Când [ H+] > [Oh− ] se spune că soluția este acidă, iar când [ Oh − ] > [H+] - alcalin.
Pentru a face mai convenabil reprezentarea, pentru a scăpa de exponentul negativ, în loc de concentrațiile de ioni de hidrogen, se folosește logaritmul lor zecimal, care este luat cu semnul opus, care este exponentul de hidrogen - pH.
Indicele de bazicitate al unei soluții pOH.
Un pic mai puțin popular este inversul pH valoare - indicele de bazicitate a soluției, pOH, care este egal cu logaritmul zecimal (negativ) al concentrației din soluția de ioni Oh − :
ca în fiecare soluție apoasă la 25 °C, deci la această temperatură:
Valorile pH-ului în soluții de aciditate diferită.
- Contrar credinței populare, pH poate varia cu excepția intervalului 0 - 14, poate depăși și aceste limite. De exemplu, la o concentrație de ioni de hidrogen [ H+] = 10 −15 mol/l, pH= 15, la o concentrație de ioni de hidroxid de 10 mol/l pOH = −1 .
Deoarece la 25 °C (condiții standard) [ H+] [Oh − ] = 10 −14 , este clar că la această temperatură pH + pOH = 14.
Deoarece în soluții acide [ H+] > 10 −7 , ceea ce înseamnă că pentru soluții acide pH < 7, соответственно, у щелочных растворов pH > 7 , pH soluții neutre este 7. La temperaturi mai ridicate, constanta de disociere electrolitică a apei crește, ceea ce înseamnă că produsul ionic al apei crește, atunci acesta va fi neutru pH= 7 (care corespunde concentrațiilor crescute simultan ca H+, și Oh−); cu scăderea temperaturii, dimpotrivă, neutru pH crește.
Metode de determinare a valorii pH-ului.
Există mai multe metode pentru a determina valoarea pH solutii. Valoarea pH-ului este estimată aproximativ folosind indicatori, măsurați cu precizie folosind pH-metru sau determinat analitic prin efectuarea titrarii acido-bazice.
- Pentru o estimare aproximativă a concentrației de ioni de hidrogen, se utilizează adesea indicatori acido-bazici- coloranți organici, de culoarea cărora depinde pH mediu inconjurator. Cei mai populari indicatori sunt: turnesol, fenolftaleina, metil portocaliu (metil portocaliu), etc. Indicatorii pot fi sub 2 forme colorate diferit - fie acide, fie bazice. Schimbarea culorii tuturor indicatorilor are loc în intervalul lor de aciditate, adesea 1-2 unități.
- Pentru a mări intervalul de măsurare de lucru pH aplica indicator universal, care este un amestec de mai mulți indicatori. Indicatorul universal își schimbă în mod constant culoarea de la roșu la galben, verde, albastru la violet atunci când trece de la o regiune acidă la una alcalină. Definiții pH metoda indicatorului este dificilă pentru soluții tulburi sau colorate.
- Utilizarea unui dispozitiv special - pH-metru - face posibilă măsurarea pHîntr-o gamă mai largă și mai precis (până la 0,01 unități pH) decât cu indicatorii. Metoda ionometrică de determinare pH se bazează pe măsurarea EMF a unui circuit galvanic cu un milivoltmetru-ionometru, care include un electrod de sticlă, al cărui potențial depinde de concentrația de ioni. H+în soluția înconjurătoare. Metoda are precizie și comoditate ridicate, mai ales după calibrarea electrodului indicator în intervalul selectat pH, ceea ce face posibilă măsurarea pH soluții opace și colorate și, prin urmare, este adesea folosit.
- Metoda analitică volumetrică — titrare acido-bazică- oferă, de asemenea, rezultate precise pentru determinarea acidității soluțiilor. O soluție de concentrație cunoscută (titrant) este adăugată prin picurare la soluția de testat. Când sunt amestecate, reactie chimica. Punctul de echivalență - momentul în care titrantul este exact suficient pentru a finaliza reacția - este fixat cu ajutorul unui indicator. După aceea, dacă se cunosc concentrația și volumul soluției de titrant adăugate, se determină aciditatea soluției.
- pH:
0,001 mol/L acid clorhidric la 20 °C are pH=3, la 30 °C pH=3,
0,001 mol/L NaOH la 20 °C are pH=11,73, la 30 °C pH=10,83,
Influența temperaturii asupra valorilor pH explică disocierea diferită a ionilor de hidrogen (H +) și nu este o eroare experimentală. Efectul temperaturii nu poate fi compensat electronic pH-metru.
Rolul pH-ului în chimie și biologie.
Aciditatea mediului este importantă pentru majoritatea proceselor chimice, iar posibilitatea de apariție sau rezultatul unei anumite reacții depinde adesea de pH mediu inconjurator. Pentru a menține o anumită valoare pHîn sistemul de reacţie în timpul cercetare de laborator sau soluții tampon sunt utilizate în producție, permițându-vă să mențineți o valoare aproape constantă pH când este diluat sau când în soluție se adaugă cantități mici de acid sau alcali.
Indicator de hidrogen pH adesea folosit pentru a caracteriza proprietățile acido-bazice ale diferitelor medii biologice.
Pentru reacțiile biochimice, aciditatea mediului de reacție care apare în sistemele vii este de mare importanță. Concentrația ionilor de hidrogen într-o soluție afectează adesea proprietățile fizico-chimice și activitate biologică proteine si acizi nucleici Prin urmare, pentru funcționarea normală a organismului, menținerea homeostaziei acido-bazice este o sarcină de o importanță excepțională. Menținerea dinamică a optime pH fluidele biologice se realizează sub acțiunea sistemelor tampon ale organismului.
În corpul uman în diferite organe, valoarea pH-ului este diferită.
|
Unele sensuri pH. |
|
|
Substanţă |
|
|
electrolitul din bateriile cu plumb |
|
|
Suc gastric |
|
|
Suc de lămâie (soluție de acid citric 5%) |
|
|
otet alimentar |
|
|
Coca cola |
|
|
suc de mere |
|
|
Pielea unei persoane sănătoase |
|
|
Ploaie acidă |
|
|
Bând apă |
|
|
Apă pură la 25°C |
|
|
Apa de mare |
|
|
Săpun (gras) pentru mâini |
|
|
Amoniac |
|
|
Înălbitor (înălbitor) |
|
|
Soluții alcaline concentrate |
|