Vodík a oxid uhličitý sa dajú ľahko premeniť na kyselinu mravčiu a naopak. Spôsob výroby metánu a jeho derivátov Podmienky reakcie oxidu uhličitého s vodíkom
výbušné plyny, skleníkový efekt
Tento výbušný plyn sa často označuje ako „bažinový plyn“. Každý pozná jeho špecifickú vôňu, no v skutočnosti ide o špeciálne prísady „s vôňou plynu“, ktoré sa pridávajú, aby ju rozpoznali. Pri spálení prakticky nezanecháva škodlivé produkty. Okrem iného sa tento plyn pomerne aktívne podieľa na vzniku známeho skleníkového efektu.
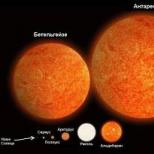
Plyn zvyčajne spojený so živými organizmami. Keď bol v atmosfére Marsu a Titanu objavený metán, vedci dúfali, že na týchto planétach existuje život. Na Červenej planéte nie je veľa metánu, ale Titan je ním doslova „naplnený“. A ak nie pre Titan, tak pre Mars sú biologické zdroje metánu rovnako pravdepodobné ako geologické. Veľa metánu je na obrích planétach – Jupiter, Saturn, Urán a Neptún, kde vznikol ako produkt chemického spracovania látky protosolárnej hmloviny. Na Zemi je vzácny: jeho obsah v atmosfére našej planéty je len 1750 častí na miliardu objemu (ppbv).
Zdroje a výroba metánu
Metán je najjednoduchší uhľovodík, bezfarebný plyn bez zápachu. Jeho chemický vzorec je CH4. Mierne rozpustný vo vode, ľahší ako vzduch. Pri použití v každodennom živote, priemysle sa do metánu zvyčajne pridávajú odoranty so špecifickým „plynovým zápachom“. Hlavnou zložkou sú prírodné (77-99%), pridružené ropné (31-90%), banské a močiarne plyny (odtiaľ ďalšie názvy pre metán - močiar alebo banský plyn).
Na 90 – 95 % má metán biologického pôvodu. Bylinožravé kopytníky, ako sú kravy a kozy, vydávajú pätinu svojich ročných emisií metánu, ktorý produkujú baktérie v žalúdku. Ďalšími dôležitými zdrojmi sú termity, nelúpaná ryža, močiare, filtrácia zemného plynu (produkt minulého života) a fotosyntéza rastlín. Sopky prispievajú k celkovej bilancii metánu na Zemi menej ako 0,2 %, ale zdrojom tohto plynu môžu byť aj organizmy z minulých období. Priemyselné emisie metánu sú zanedbateľné. Detekcia metánu na planéte ako je Zem teda naznačuje prítomnosť života na nej.
Metán vzniká pri tepelnom spracovaní ropy a ropných produktov (10-57 % obj.), koksovaní a hydrogenácii uhlia (24-34 %). Laboratórne metódy získavania: fúzia octanu sodného s alkáliou, pôsobenie vody na metylmagnéziumjodid alebo na karbid hliníka.
Pripravuje sa v laboratóriu zahrievaním sodného vápna (zmes hydroxidu sodného a draselného) alebo bezvodého hydroxidu sodného s kyselinou octovou. Pre túto reakciu je dôležitá neprítomnosť vody, preto sa používa hydroxid sodný, pretože je menej hygroskopický.
Vlastnosti metánu
horieť vo vzduchu modrastý plameň, pričom sa uvoľní energia cca 39 MJ na 1m 3 . Formuje sa vzduchom výbušné zmesi. Zvlášť nebezpečný je metán uvoľňovaný pri podzemnej ťažbe ložísk nerastných surovín do banských diel, ako aj v úpravniach uhlia a brikiet, v triediarňach. Takže pri obsahu do 5-6% vo vzduchu horí metán v blízkosti zdroja tepla (teplota vznietenia 650-750°C), od 5-6% do 14-16% exploduje, viac ako 16% môže horieť s prílevom kyslíka zvonku. Pokles koncentrácie metánu v tomto prípade môže viesť k výbuchu. Okrem toho výrazné zvýšenie koncentrácie metánu vo vzduchu spôsobuje zadusenie (napríklad koncentrácia metánu 43 % zodpovedá 12 % O 2).Výbušné spaľovanie sa šíri rýchlosťou 500-700 pani; tlak plynu pri výbuchu v uzavretom objeme je 1 MN/m2. Po kontakte so zdrojom tepla dochádza k vznieteniu metánu s určitým oneskorením. Táto vlastnosť je založená na vytvorení bezpečnosti výbušniny a elektrické zariadenia v nevýbušnom prevedení. Na lokalitách, ktoré sú nebezpečné prítomnosťou metánu (hlavne uhoľné bane), tzv. plynový režim.
Pri 150–200 °C a tlaku 30–90 atm sa metán oxiduje na kyselina mravčia.
Metán tvorí inklúzne zlúčeniny - plynové hydráty, široko rozšírené v prírode.
Aplikácia metánu
Metán je tepelne najstabilnejší nasýtený uhľovodík. Je široko používaný ako domáce a priemyselné palivo A ako suroviny pre priemysel. Chloráciou metánu sa teda vyrába metylchlorid, metylénchlorid, chloroform, tetrachlórmetán.
Nedokonalým spaľovaním vzniká metán sadze počas katalytickej oxidácie - formaldehyd, pri interakcii so sírou - sírouhlík.
Tepelno-oxidačné krakovanie A elektrokrakovanie metán - dôležité priemyselné metódy získavania acetylén.
Základom priemyselnej výroby je katalytická oxidácia zmesi metánu a amoniaku kyselina kyanovodíková. Metán sa používa ako zdroj vodíka pri výrobe amoniaku, ako aj na výrobu vodného plynu (tzv. syntézneho plynu): CH 4 + H 2 O → CO + 3H 2, používaného na priemyselnú syntézu uhľovodíkov, alkoholov, aldehydov atď. Dôležitým derivátom metánu je nitrometán.
Automobilové palivo
Metán je široko používaný ako motorové palivo pre automobily. Hustota prírodného metánu je však tisíckrát nižšia ako hustota benzínu. Ak teda naplníte auto metánom pri atmosferický tlak, potom na rovnaké množstvo paliva s benzínom budete potrebovať nádrž 1000-krát väčšiu. Aby sa nevozil obrovský príves s palivom, je potrebné zvýšiť hustotu plynu. To sa dá dosiahnuť stlačením metánu na 20-25 MPa (200-250 atmosfér). Na skladovanie plynu v tomto stave sa používajú špeciálne fľaše, ktoré sú inštalované na autách.
Metán a skleníkový efekt
Metán je skleníkový plyn. Ak miera vplyvu oxid uhličitý na klímu podmienečne branú ako jednotku, potom skleníková aktivita metánu bude 23 jednotiek. Obsah metánu v atmosfére za posledné dve storočia veľmi rýchlo vzrástol.
Teraz sa priemerný obsah metánu CH 4 v modernej atmosfére odhaduje na 1,8 ppm ( časti na miliónčasti na milión). A hoci je to 200-krát menej ako obsah oxidu uhličitého (CO 2) v ňom, na molekulu plynu sa skleníkový efekt metánu – teda jeho príspevok k rozptylu a zadržiavaniu tepla vyžarovaného Zemou ohrievanou slnko - je podstatne vyššia ako z CO 2 . Metán navyše pohlcuje žiarenie Zeme v tých „oknách“ spektra, ktoré sú priehľadné pre iné skleníkové plyny. Bez skleníkových plynov – CO 2 , vodnej pary, metánu a niektorých ďalších nečistôt by bola priemerná teplota na povrchu Zeme len -23°C a teraz je okolo +15°C.
Metán presakuje trhlinami na dne oceánu zemská kôra, sa uvoľňuje v značných množstvách pri ťažbe a pri vypaľovaní lesov. Nedávno objavili nový, úplne neočakávaný zdroj metánu - vyššie rastliny, ale mechanizmy vzniku a význam tohto procesu pre samotné rastliny ešte neboli objasnené.

Metán na Zemi

V blízkosti Santa Barbary sa z dna oceánu vo veľkých objemoch vypúšťa metán, aktívny skleníkový plyn, vo forme bublín.

Metán je obzvlášť nebezpečný pri banských prácach.

Metán namiesto benzínu? Jednoducho

Keď bol v atmosfére Marsu objavený metán, vedci dúfali, že na planéte nájdu stopy života.
Vo svete skolaudovaných závodov na výrobu metánu z dreva je zatiaľ len niekoľko realizovaných projektov. Prvé výsledky nám umožňujú dúfať v seriózny prielom v tomto smere.
Vzorce pre článok „Metán z biomasy“, viď
Metán CH 4 je bezfarebný plyn bez zápachu, ktorý je takmer dvakrát ľahší ako vzduch. V prírode vzniká v dôsledku rozkladu bez prístupu vzduchu zvyškov rastlinných a živočíšnych organizmov. Preto sa vyskytuje napríklad v močaristých nádržiach a uhoľných baniach. Metán sa nachádza vo významných množstvách v zemnom plyne, ktorý sa v súčasnosti široko používa ako palivo v každodennom živote av priemysle.
Jednou z najrýchlejšie rastúcich technológií obnoviteľnej energie v súčasnosti je výroba anaeróbneho fermentovaného biometánu a jeho následné privádzanie do sietí, ktoré dodávajú zemný plyn spotrebiteľom. Napriek vysokým nákladom na výrobu biometánu touto technológiou (8-10 eurocentov za 1 kWh) počet inštalácií na jeho výrobu neustále rastie. V roku 2009 bolo v Nemecku v prevádzke už 23 klasických (hnojových) bioplynových staníc s dodávkami plynu do existujúcich plynovodov a 36 ďalších je vo výstavbe alebo plánovaní. Dôvodom rastu tohto ukazovateľa je zákon o obnoviteľnej energii (Erneuerbare Energien Gesetz - EEG), prijatý v Nemecku v roku 2004, novelizovaný v roku 2009 a umožňujúci predajcom plynu ponúkať svojim zákazníkom plyn získaný z obnoviteľných zdrojov a získavať štátne dotácie na výrobu elektriny z obnoviteľných zdrojov energie (OZE).
Prvý závod na svete na výrobu zemného plynu z dreva v r
rakúske mesto Güssing. V popredí je jednotka na výrobu metánu
Podľa klasickej a dnes už široko používanej schémy sa biometán získava z rastlinných substrátov (napríklad kukurica), hnojovice z komplexov ošípaných, maštaľného hnoja, slepačieho hnoja a pod. Takýto metán z biomasy možno získať jej anaeróbnym rozkladom (fermentáciou). . Počas anaeróbnej digescie organickej hmoty(prírodný odpad) sa rozkladajú bez prítomnosti kyslíka. Tento proces prebieha v troch etapách, ktoré zahŕňajú dve rôzne skupiny baktérie. V prvej fáze komplexné Organické zlúčeniny(mastné kyseliny, bielkoviny, sacharidy) sa v dôsledku enzymatickej hydrolýzy premieňajú na jednoduchšie zlúčeniny. V druhom kroku sú jednoduché zlúčeniny vystavené skupine anaeróbnych (alebo kyseliny produkujúcich) baktérií, čo vedie k tvorbe hlavne prchavých mastných kyselín. V tretej fáze sa organické kyseliny pôsobením striktne anaeróbnych (alebo metán produkujúcich) baktérií premieňajú na oxid uhličitý a metán. Po tejto fáze sa získa plyn obohatený o metán (bioplyn), ktorého výhrevnosť je 5340-6230 kcal/m 3 .
Ersatzgas z pevnej biomasy, ako je drevo, má značnú výhodu oproti bioplynu získanému z hnoja, hnoja: tí, ktorí sa podieľajú na výrobe takéhoto plynu, majú k dispozícii pôsobivé objemy odpadu z pílenia, ťažby dreva a spracovania dreva. Navyše na európskom trhu sa ceny piliarskeho a drevospracujúceho odpadu, na rozdiel od cien poľnohospodárskych produktov, ktoré sa používajú na výrobu bioplynu, pohybujú oveľa menej. Nesmieme zabúdať, že používanie poľnohospodárskych produktov (obilia, kukurice, repky atď.) na výrobu bioplynu v konečnom dôsledku vedie k vyšším cenám na potravinových trhoch. Odpadové teplo z chemickej reakcie má navyše vyššiu teplotu ako odpadové teplo z fermentačných reakcií v klasických bioplynových staniciach. Z toho vyplýva, že tepelnú energiu uvoľnenú pri procesoch metanizácie dreva možno efektívnejšie využiť v regionálnom zásobovaní teplom. Dôležité je aj to, že na rozdiel od klasických bioplynových staníc nedochádza pri prevádzke zariadení na výrobu metánu z dreva k nepríjemným zápachom. Tieto inštalácie navyše zaberajú oveľa menej miesta ako klasické a môžu byť umiestnené v rámci mestských aglomerácií.
technológie

Výsledkom dnes bežne používanej metódy fermentácie (anaeróbnej fermentácie) na výrobu biometánu z poľnohospodárskych substrátov je biometán, ktorý pozostáva prevažne z metánu a oxidu uhličitého. Biometán potom musí prejsť špeciálnou úpravou a zušľachťovaním na kvalitu zemného plynu separáciou CO 2 . Tepelné straty počas fermentácie obmedzujú stupeň účinnosti celého procesného reťazca. Účinnosť je 50-60%.
Pri výrobe syntetického zemného plynu (Substitute Natural Gas - SNG) z tuhého paliva obsahujúceho uhlík, ako je uhlie alebo biomasa (drevo), sa po tepelnom splyňovaní v prvej fáze procesu získava tzv. z ktorého sa po očistení od všetkých druhov nečistôt (hlavne od oxidu uhličitého a zlúčenín síry a chlóru) syntetizuje metán. Tento exotermický proces prebieha pri teplote 300 až 450 °C a tlaku 1 až 5 bar v prítomnosti vhodného katalyzátora. V tomto prípade dochádza k nasledujúcim reakciám:
Pozrite si vzorce v
Na rozdiel od anaeróbnej fermentácie dosahuje termické splyňovanie biomasy vyššiu účinnosť, pretože odpadové teplo z výroby SNG je možné vždy využiť na mieste.
V zásade je výroba metánu zo syntézneho plynu, ako aj z plynných zmesí vodíka (H 2) a oxidu uhoľnatého (CO) veľmi stará technológia. Francúzsky chemik Paul Sabatier vynašiel metódu výroby metánu, ktorá je po ňom pomenovaná: Sabatierova reakcia alebo Sabatierov proces (fr. Sabatier-Reaktion). V roku 1912 za to dostal nobelová cena v oblasti chémie. Tento proces je reakciou vodíka s oxidom uhličitým pri zvýšenej teplote a tlaku v prítomnosti niklového katalyzátora za vzniku metánu. Ruténium s oxidom hlinitým možno použiť ako účinnejší katalyzátor.
Proces je opísaný nasledujúcou chemickou reakciou:
C02 + 4H2 -> CH4 + 2H20.
Pretože obe reakcie sú vysoko exotermické, bez špeciálnych opatrení na chladenie reaktorov alebo recirkuláciu by sa pri zahriatí na 600 °C katalyzátor zničil. Pri vysokých teplotách sa navyše posúva termodynamická rovnováha H 2 a CO, takže dostatočne vysoký výťažok metánu možno dosiahnuť len pri teplotách pod 300 °C.
Technológia splyňovania bola vytvorená už v roku 1800 na výrobu syntetického plynu, ktorý je potrebný na osvetlenie miest a tiež sa používa ako nosič tepla pre domáce a priemyselné účely (hutníctvo, parné stroje atď.). Uhlie aj rastlinná biomasa a produkty jej spracovania (drevené uhlie) boli podrobené splyňovaniu.
Na výrobu syntetiky použite základný proces splyňovania uhlia chemických látok a palivá začali v 20. rokoch 20. storočia na Inštitúte cisára Wilhelma pri štúdiu uhlia v meste Mülheim-on-the-Ruhr (Nemecko). V tomto ústave vynašli Franz Fischer a Hans Tropsch spôsob výroby syntézneho plynu (syngas) na výrobu kvapalného paliva z uhlia v Nemecku. Fischer-Tropschov proces alebo Fischer-Tropschova syntéza (FTS) je chemická reakcia, prúdiaci v prítomnosti katalyzátora (železo, kobalt), v ktorom sa zmes oxidu uhoľnatého (CO) a vodíka (H 2), čiže syntézny plyn, premieňa na rôzne kvapalné uhľovodíky. Výsledné uhľovodíky sa čistia, čím sa získa cieľový produkt – syntetický olej. Oxid uhličitý a oxid uhoľnatý vznikajú pri čiastočnej oxidácii uhlia a/alebo drevného paliva.
Fischer-Tropschov proces je opísaný nasledujúcou chemickou rovnicou:
CO + 2H2 -> -CH2- + H20
2CO + H2 -> -CH2- + C02.
Syngas získaný po splyňovaní uhlia alebo pevných uhlíkatých odpadov sa môže priamo použiť ako palivo bez ďalšej konverzie Fischer-Tropschovým procesom. Prechod z plynného paliva na kvapalné palivo je teda celkom jednoduchý. Počas druhej svetovej vojny v Nemecku sa Fischer-Tropschova syntéza používala v ôsmich závodoch na výrobu syntetickej motorovej nafty (asi 600 tisíc ton ročne). Projekt bol plne financovaný štátom. Po skončení druhej svetovej vojny v Nemecku boli všetky tieto továrne zatvorené a čiastočne spolu s technikou vyvezené ako reparácie do USA a odtiaľ sa rozišli do sveta. V Juhoafrickej republike zároveň spoločnosť South African Synthetic Oil Ltd. (SASOL), s využitím nemeckej technológie, začala vyrábať syntetické palivá a dodnes vo svojich štyroch závodoch v Južnej Afrike a jednom závode v Katare produkuje viac ako 200 tisíc barelov ropného ekvivalentu kvapalných uhľovodíkov ročne. Južná Afrika je už dlho jedinou krajinou na svete, ktorá vyvinula proces SFT. Po kríze v roku 1973 však svetové ropné a energetické spoločnosti v mnohých krajinách (najmä USA a Nemecku) začali prejavovať záujem tak o výrobu syntetických kvapalných palív, ako aj o výrobu zemného syntézneho plynu.
Bolo vypracovaných množstvo projektov na výrobu zemného syntézneho plynu, ale iba jeden z nich bol úspešne realizovaný v priemyselnom meradle. V roku 1984 bola v Spojených štátoch spustená továreň na metanizáciu hnedého uhlia Great Plains Synfuels Plant (Dakotagas Company), ktorá dodnes vyrába syntetický zemný plyn dodávaný do siete, cez ktorú sa prepravuje zemný plyn. Denná kapacita závodu je 3,9 milióna m 3 SNG.
Zážitok je vhodné pripomenúť Sovietsky zväz, kde od konca 20. do 50. rokov 20. storočia fungovali plynové generátory využívajúce drevo (palivové drevo a drevené uhlie) a rašelinu na výrobu plynného motorového paliva. V roku 1929 bola v ZSSR postavená prvá veľká plynárenská stanica pracujúca na rašeline a v nasledujúcich rokoch bolo vybudovaných niekoľko ďalších podobných staníc vo veľkých podnikoch. Výroba drevoplynu sa využívala najmä ako palivo v doprave. Po začatí rozvoja západnej Sibíri a objavení najväčších svetových ložísk modrého paliva sa na výrobu plynu v ZSSR, žiaľ, nezaslúžene zabudlo.
Získavanie metánu z dreva
Pri splyňovaní sa biomasa s chemický vzorec CH n O m sa najskôr premení na syntézny plyn, pozostávajúci z vodíka a oxidu uhoľnatého. Zo stechiometrického všeobecná rovnica metanizačné reakcie biomasy so sumárnym vzorcom
CH 1,23 O 0,38 + 0,5025 H20 → 0,55875 CH4 + 0,44125 C20
z toho vyplýva, že do metánového reaktora treba privádzať vodu alebo vodnú paru a odvádzať z neho oxid uhličitý. Tu je viacero možností: buď sa CO 2, ako pri priemyselnej syntéze, odstraňuje zo syntézneho plynu priamo z metánového reaktora, alebo ako pri príprave bioplynu (fermentácia) po procese metanizácie už z nerafinovaného syntetického zemného plynu. . Výhodou prvej metódy oproti ostatným je, že už vyčistený plyn vstupuje do metanačného cyklu. Výhody druhého spôsobu spočívajú v tom, že metánový reaktor môže pracovať s prebytkom vodnej pary, čo výrazne znižuje tvorbu uhlíka.
V týchto oblastiach sa pracuje v Inštitúte Paula Scherrera (Švajčiarsko), ktorý sa podieľal najmä na písaní Programu výroby metánu z biomasy pomocou nových technológií (v katalyticky aktívnych vortexových vrstvách) v rámci projektu EU BioSNG . Táto technológia bola uvedená do praxe v tepelnej elektrárni v rakúskom meste Gussing. Zariadenie na syntézu metánu, ktoré bolo uvedené do prevádzky v roku 2009, má výkon 1 MW a funguje na drevnú štiepku. Vo švédskom Göteborgu sa v súčasnosti diskutuje o projekte 30 MW dreveného metánu. Podobné práce sa vykonávajú v Nemecku (Stuttgart, ZSW), Holandsku (Centrum energetického výskumu, ECN) a na Inštitúte tepelného inžinierstva Technická univerzita v Grazi (Rakúsko) v spolupráci s Agnion v Pfaffenhofen an der Ilm (Nemecko).
Účinnosť syntézy metánu z biomasy
Pri príjme metánu v každej fáze procesu, ako pri každom procese syntézy, sú straty nevyhnutné. Pri exotermických reakciách sa odoberá teplo, ktorého energetický obsah nemôže byť v konečnom produkte syntézy väčší ako chemicky viazaná energia počas procesu syntézy. Pre metanizáciu to znamená, že len asi 60 % energie použitej biomasy je uložených v hotovom produkte – SNG.
Ale keďže odoberané teplo má vysokú teplotu – od 200 do 400 °C, dá sa použiť na mieste. Z tohto dôvodu sú malé zariadenia na syntézu metánu obzvlášť ziskové, pretože je možné vyriešiť problém využitia odpadového tepla o 100%, napríklad na vykurovanie domácností, fariem, aplikácie v sušiarňach atď. využiť nielen odpadové teplo z procesov splyňovania a metanizácie, ale aj kondenzačné teplo vodnej pary v nerafinovanom syngase, ktorý obsahuje až 50 % vodnej pary. Celková účinnosť pri takomto plnom využití tepla a predaji výsledného SNG do plynárenskej siete a zásobníka plynu sa blíži k 95 %. Návratnosť takýchto projektov je len niekoľko rokov.
Vzhľadom na to, že zemný plyn je možné vždy využívať s oveľa vyššou účinnosťou ako tuhé palivá z biomasy, je rozumnejšie používať metán získaný z dreva ako priamo spaľovať tuhé biopalivá. Dôvod: pri využití zemného plynu na výrobu elektriny v elektrárni s plynovou alebo parnou turbínou sa získava až 60 % elektriny a pri spaľovaní tuhého paliva z biomasy je veľmi ťažké realizovať projekty s výťažnosťou elektriny nad 30 %. Pri decentralizovanej výrobe elektriny do 1 MW/h sú tiež plynové kogeneračné elektrárne využívajúce syntézny plyn efektívnejšie ako tepelné elektrárne využívajúce organický cyklický proces (ORC proces) a spaľujúce tuhé biopalivá.
Prevádzka takýchto tepelných elektrární je založená na slede cyklov procesu termodynamickej cirkulácie (ORС - organický Rankinov cyklus) pracovnej tekutiny s vysokým molekulovej hmotnosti(termálny olej, organické odparujúce sa látky). Obehové čerpadlo čerpá pracovnú kvapalinu do výmenníka tepla vysokoteplotného organického chladiva, kde sa odparuje. Kvapalné pary poháňajú turbínu, po ktorej vstupujú do ďalšieho výmenníka tepla, kde ochladzované vodou alebo vzduchom kondenzujú. Kondenzát vstupuje do kolektora obehového čerpadla a termodynamický cyklus (ORC) sa opakuje. Chladiaca kvapalina ani chladiaca kvapalina nie sú v priamom kontakte s turbínou alebo pracovnou kvapalinou. Procesom ORC dosahujú tepelné elektrárne vysoký výkon, prevádzkovú spoľahlivosť a hospodárnosť.
Aj výroba len jednej tepelnej energie pomocou biometánu je konkurencieschopná konvenčným spôsobom výroby tepla. Ak sa odpadové teplo z procesu metanizácie dreva využije na mieste (decentralizované) a vyrobený plyn smeruje do zásobníka zemného plynu, získa sa celková miera využitia 93 %, čo napríklad tepelné elektrárne využívajúce drevnú štiepku resp. pelety nedosahujú (účinnosť samotného zariadenia je nižšia a navyše dochádza k stratám v tepelných sieťach).
Spolu s pripraveným syntéznym plynom rovnakej kvality ako zemný plyn môžu veľké plynové tepelné elektrárne využívať na spoluspaľovanie so zemným plynom aj „surový“ syntézny plyn, čím sa výrazne znížia náklady na vyrobenú energiu.
Plyn z biomasy alebo fosílny zemný plyn?
Syntetický zemný plyn (SNG) je čistený syntetický plyn, ktorý má rovnaké vlastnosti ako zemný plyn.
Náklady na výrobu SNG z drevnej štiepky v závodoch do 1 MW sú podľa prepočtov Agnionu 8-10 eurocentov/kWh.
Náklady na výrobu biometánu sú porovnateľné s nákladmi na ťažbu a prepravu fosílneho zemného plynu. Takáto výroba je však zatiaľ nekonkurencieschopná. Všetko bude závisieť od svetových cien ropy. Ak je cena ropy napríklad 100 dolárov za barel, tak v Nemecku je pre priemyselných zákazníkov cena zemného plynu 5-6 eurocentov/kWh. Pre súkromné domácnosti bude cena vyššia – 8-10 eurocentov/kWh. Pri opakovane predpovedanej cene ropy viac ako 200 dolárov za barel by zemný plyn stál aj priemyselných zákazníkov trvalo viac ako 10 centov/kWh. Za tejto podmienky by výroba SNG z biomasy mohla byť ekonomicky životaschopná aj bez dotácií podľa zákona o OZE. A na Ukrajine sa pri súčasných cenách získava syntézny plyn za polovičnú cenu zemného plynu. Vyvíjajú vlastný projekt na získavanie syntézneho plynu splyňovaním zmesi pilín, slamy, rašeliny a uhlia. Jeho zloženie: až 25-30% metánu, 30-35% oxidu uhoľnatého a zvyšných 6% - dusík a oxid uhličitý.
V súčasnosti energetické potreby sveta predstavujú približne 11 – 12 miliárd ton štandardného paliva (cf) a ropa a plyn ich uspokojujú na 58 – 60 %. Zdroje každoročne obnoviteľnej rastlinnej biomasy sú energeticky 25-krát vyššie ako objem vyprodukovanej ropy. V súčasnosti tvorí spálená rastlinná biomasa približne 10 % spotrebovaných energetických zdrojov (cca 1 miliarda ton palivového ekvivalentu), v budúcnosti dôjde k výraznému rozšíreniu využitia biomasy vo forme produktov jej spracovania (kvapalné, tuhé palivá a pod.) a v prvom rade sa očakáva odpad, ktorý sa hromadí a rozkladá, čím znečisťuje životné prostredie.
Zvýši sa dopyt po rope a zemnom plyne a zároveň sa zlepší energetické využitie rastlinnej biomasy (okrem jej priameho spaľovania). Iste, v tejto nádhernej budúcnosti bioenergie budú vyššie uvedené technológie žiadané na úplne inej, priemyselnej úrovni. V každom prípade tomu chcem veriť.
Sergei PEREDERIY,
EKO Holz-und Pellethandel GmbH,
Düsseldorf, Nemecko
Získavanie metánu z oxidu uhličitého je proces, ktorý si vyžaduje laboratórne podmienky. Takže v roku 2009 na Pensylvánskej univerzite (USA) sa metán vyrábal z vody a oxidu uhličitého pomocou nanorúriek pozostávajúcich z TiO 2 (oxid titaničitý) a obsahujúcich prímes dusíka. Na získanie metánu vedci umiestnili vodu (v parnom stave) a oxid uhličitý do kovových nádob, ktoré boli zvnútra uzavreté vekom s nanorúrkami.
Proces získavania metánu je nasledovný - pod vplyvom slnečného svetla sa vo vnútri trubíc objavili častice, ktoré nesú nabíjačka. Takéto častice rozdelili molekuly vody na vodíkové ióny (H, ktoré sa potom zlúčili do vodíkových molekúl H 2) a hydroxylové radikály (častice -OH). Ďalej sa v procese získavania metánu oxid uhličitý rozdelil na oxid uhoľnatý (CO) a kyslík (02). Nakoniec oxid uhoľnatý reaguje s vodíkom za vzniku vody a metánu.
Reverzná reakcia - tvorba oxidu uhličitého nastáva v dôsledku parnej deformácie metánu - pri teplote 700-1100 ° C a tlaku 0,3-2,5 MPa.
Vedúci Inštitútu priemyselných vied na Tokijskej univerzite, Národný inštitút veda a pokročilé technológie (National Institute of Advanced Industrial Science and Technology, AIST), Hitachi Zosen Corp, JGC Corp a EX Research Institute Ltd sa 18. novembra 2016 rozhodli zorganizovať novú spoločnú výskumnú skupinu „CCR (carbon capture & reuse ) Study Skupina“. Táto skupina bude vyvíjať rozsiahle technológie, ktoré dokážu vyrábať kvapalné a plynné palivá, ako je metán, pomocou atmosférického oxidu uhličitého a vodíka vyrobeného elektrolýzou s využitím energie z čistých obnoviteľných zdrojov.
Táto skupina sa zameria predovšetkým na výskum zameraný na zvyšovanie efektívnosti využívania energie z obnoviteľných zdrojov, efektívnosť technológií získavania oxidu uhličitého z atmosféry a jeho ďalšie využitie a vývoj nových modernejších metód získavania vodíka z vody elektrolýza.
Budúce technológie budú založené na pomerne dobre známych fyzikálnych procesoch a chemických transformáciách realizovaných na modernej technologickej úrovni. Oxid uhličitý uvoľnený do atmosféry pri spaľovaní akéhokoľvek typu fosílneho paliva bude reagovať s vodíkom. Tento vodík sa bude získavať elektrolýzou a na to potrebná energia bude pochádzať výlučne z ekologických zdrojov, predovšetkým zo solárnych a veterných elektrární.
Táto technológia je považovaná nielen za čistý zdroj kvapalných a fosílnych palív. Ďalšou funkciou tejto technológie bude akumulácia vo forme paliva prebytočnej energie prijatej zo solárnych a veterných elektrární počas hodín jej minimálnej spotreby.
Skupina CCR sa bude zaoberať všetkými existujúcimi formami obnoviteľnej čistej energie. Navyše nový efektívne metódy produkovať vodík, uvoľňovať oxid uhličitý a premieňať ho na palivo.
Práca na všetkých skúmaných a vyvíjaných technológiách bude prebiehať z dvoch pozícií. Prvou pozíciou bude vytvorenie malých, prípadne mobilných zariadení s nie príliš veľkou kapacitou, ktoré dokážu zabezpečiť potreby samostatnej malej skupiny ľudí s metánovým plynom (decentralizovaný model). A druhým smerom bude rozvoj rozsiahlych výrobných systémov, ktoré budú mať dostatočne vysokú kapacitu a ktoré možno zaradiť do všeobecnej energetickej siete krajiny (centralizovaný model).
Kyselina mravčia, ktorej vzorec je HCOOH, je najjednoduchšia monokarboxylová kyselina. Ako je zrejmé z jeho názvu, zdrojom jeho objavu sa stali charakteristické sekréty červených mravcov. Dotyčná kyselina je súčasťou jedovatej látky, ktorú vylučujú bodavé mravce. Obsahuje aj horiacu tekutinu, ktorú tvoria bodavé húsenice priadky morušovej.
Prvýkrát sa roztok kyseliny mravčej získal pri pokusoch slávneho anglického vedca Johna Raya. Na konci sedemnásteho storočia zmiešal v nádobe vodu a červené drevené mravce. Potom sa nádoba zahriala do varu a cez ňu prechádzal prúd horúcej pary. Výsledkom experimentu bolo získať vodný roztok, ktorého charakteristickou črtou bola silne kyslá reakcia.
V polovici osemnásteho storočia sa Andreasovi Sigismundovi Marggrafovi podarilo získať čistú kyselinu mravčiu. Bezvodá kyselina, ktorú získal nemecký chemik Justus Liebig, je považovaná za najjednoduchšiu a zároveň najsilnejšiu karboxylovú kyselinu. Podľa modernej nomenklatúry sa nazýva kyselina metanová a ide o mimoriadne nebezpečnú zlúčeninu.
K dnešnému dňu sa získavanie prezentovanej kyseliny uskutočňuje niekoľkými spôsobmi, vrátane niekoľkých po sebe nasledujúcich etáp. Ale je dokázané, že vodík a oxid uhličitý sa dokážu premeniť na kyselinu mravčiu a vrátiť sa do pôvodného stavu. Vývoj tejto teórie vykonali nemeckí vedci. Relevantnosť témy bola minimalizovať príjem oxidu uhličitého do atmosférický vzduch. Tento výsledok je možné dosiahnuť jeho aktívnym využívaním ako hlavného zdroja uhlíka pre syntézu organických látok.
Inovatívna technika vyvinutá nemeckými špecialistami zahŕňa realizáciu katalytickej hydrogenácie s tvorbou kyseliny mravčej. Podľa nej sa oxid uhličitý stáva základným materiálom aj rozpúšťadlom na separáciu finálny produkt pretože reakcia prebieha v superkritickom CO2. Vďaka tomuto integrovanému prístupu sa výroba kyseliny metánovej v jednom kroku stáva realitou.
Proces hydrogenácie oxidu uhličitého za vzniku kyseliny metánovej je v súčasnosti jedným z objektov aktívneho výskumu. Hlavným cieľom vedcov je získavanie chemických zlúčenín z odpadových produktov, ktoré vznikajú v dôsledku spaľovania fosílnych palív. Okrem širokej distribúcie kyseliny mravčej v rôznych priemyselných odvetviach je potrebné poznamenať jej účasť na skladovaní vodíka. Je možné, že úlohu paliva pre vozidlá vybavené solárnymi panelmi zohrá práve táto kyselina, z ktorej možno katalytickými reakciami extrahovať vodík.
Vznik kyseliny metánu z oxidu uhličitého homogénnou katalýzou je predmetom skúmania odborníkov od 70. rokov minulého storočia. Hlavným problémom je posun rovnováhy smerom k východiskovým materiálom, ktorý sa pozoruje v štádiu rovnovážnej reakcie. Na vyriešenie problému je potrebné odstrániť kyselinu mravčiu zo zloženia reakčnej zmesi. Ale v súčasnosti sa to dá dosiahnuť iba vtedy, ak sa metánová kyselina premení na soľ alebo inú zlúčeninu. Preto je možné získať čistú kyselinu iba v prítomnosti dodatočného stupňa, ktorý spočíva v zničení tejto látky, čo neumožňuje dosiahnuť organizáciu neprerušeného procesu tvorby kyseliny mravčej.
Čoraz populárnejší je však unikátny koncept, ktorý vyvíjajú vedci zo skupiny Walter Leitner. Naznačujú, že integrácia stupňov hydrogenácie oxidu uhličitého a izolácia produktu s ich implementáciou v tom istom zariadení umožňuje, aby bol proces získavania čistej kyseliny metánu neprerušovaný. Ako sa vedcom podarilo dosiahnuť maximálnu efektivitu? Dôvodom bolo použitie dvojfázového systému, v ktorom mobilnú fázu predstavuje nadkritický oxid uhličitý a stacionárnu fázu predstavuje iónová kvapalina, tekutá soľ. Je potrebné poznamenať, že iónová kvapalina sa použila na rozpustenie katalyzátora aj zásady na stabilizáciu kyseliny. Prúdenie oxidu uhličitého v podmienkach, keď tlak a teplota prekračujú kritické hodnoty, prispieva k odstráneniu kyseliny metánu zo zloženia reakčnej zmesi. Je dôležité, aby prítomnosť superkritického oxidu uhličitého neviedla k rozpusteniu iónových kvapalín, katalyzátora, bázy, čím sa zabezpečí maximálna čistota výslednej látky.